단백질의 불소화에 따른 단백질의 언폴딩 측정
내인성 형광은 단백질 구조와 기능의 강력한 지표다.형광의 양은 종종 온도, pH 및 이온 농도의 변화를 포함한 다른 생물학적 조건 하에서 단백질의 형태 상태 또는 활성에 대한 연구자의 통찰력을 줄 수 있습니다.
Introduction
형광 측정을 위해서는 신뢰할 수 있는 여기 소스가 필요하다. 발광 다이오드(LED)는 이러한 측정에 비용 효율적인 선택이며, 오늘날 단백질과 아미노산에 대한 귀중한 정보를 산출하는 데 사용할 수 있는 고출력 UV LED를 사용할 수 있다.
이를 증명하기 위해, 우리는 LLS 시리즈 280 nm UV LED와 QE 시리즈 백박형 CCD 어레이 분광계(이 응용을 위한 전형적인 선택은 QE Pro-FL 모델)를 사용하여 리소자임과 보빈 세럼 알부민(BSA)의 샘플로부터 서로 다른 형태 상태에서 고유 형광을 측정하였다. Lysozyme은 박테리아 제제로 자주 사용되는 자연 발생 효소입니다. BSA는 신체의 생화학적 기능에 중요한 단백질입니다.이 결과는 단백질의 형광을 모니터링하는 모듈식 분광법의 힘을 보여 주었으며, 구성 요소 간의 유연성으로 인해 사용자가 생체 분자 및 심지어 형광에 UV 여기가 필요한 비 생물학적 샘플에 대한 설정을 구성할 수 있습니다.
Background
대부분의 단백질은 UV광으로 여기될 때 형광을 내는 방향족 아미노산으로 구성된다. 샘플의 형광 스펙트럼은 단백질의 아미노산 조성과 형태 상태에 따라 달라진다. 단백질이 토종(접힌)에서 변성(접지 않은) 상태로 이동함에 따라 방향족 아미노산을 둘러싼 지역 환경이 변하여 산의 형광 특성에 영향을 미친다. 이러한 고유 단백질 형광의 변화는 단백질의 전개를 감시하는데 사용될 수 있다. 이것은 오늘날 연구자들이 부적절한 단백질 전개와 관련된 신경 퇴행성 질환 및 기타 조건을 조사하는 의학 진단과 같은 응용 분야에 유용한 정보입니다.
단백질의 고유 상태는 상승된 온도, 우레아 또는 구아니딘 염산염과 같은 카오트로픽 또는 기타 화학 제제 및 pH 조절을 사용하여 변경 될 수 있습니다. 단백질이 전개됨에 따라 이전에 단백질의 소수성 코어에 묻혀 있던 아미노산이 용매에 노출됩니다.용매 노출 및 그에 따른 담금질제에 대한 감수성은 트립토판(Trp), 티로신(Tyr) 및 페닐알라닌(Phe)의 형광을 감소시킨다.
Measurement Conditions
280 nm UV LED는 고감도 분광계와 함께 라이소자임과 BSA 샘플의 형광을 측정하기 위해 사용되었습니다. 단백질의 형태에 미치는 영향을 알아보기 위해, 인산염 완충 식염수(1X PBS pH 7.4)와 0.1 M HCl/KCl(pH 1)에 희석된 단백질에 대해 형광 스펙트럼을 측정하였다.
시료는 1X PBS와 0.1 M HCl/KCl에서 3 mg/mL lysozyme (L6876 Sigma)과 12 mg/mL BSA (A2153 Sigma)를 제조하였다. PBS는 일관된 시료 pH를 유지하기 위해 사용되는 완충액이다. 1X PBS에 정지된 단백질은 고유(접힌) 상태에 머물러야 한다. 단백질이 낮은 pH 0.1 M HCl / KCl 용액에 현탁됨에 따라 단백질은 변성되기 시작하여 이전에 단백질의 코어 내에 함유된 아미노산을 용매 환경에 노출시킵니다.
탈이온수에 5 mg/mL L-Tryptophan (T90204 Aldrich) 용액을 제조하여 흡광도 측정을 통해 트립에 대한 최적의 여기 파장을 결정하고 트립 형광에 대한 기준을 제공하였다.형광과 흡광도 측정을 모두 수행하였다.
Results
Trp는 고유 단백질 형광 스펙트럼의 주요 기여자이며 방향족 아미노산의 가장 높은 양자 수율을 가지고 있습니다. Trp 흡광도 스펙트럼은 Trp의 인돌 그룹으로부터 발생하는 ~280 nm에서 피크를 갖는다. 280 nm LED에 의해 여기된 형광 스펙트럼은 ~350 nm에서 피크를 갖는다. Tyr은 274 nm 부근에서 최적의 여기를 갖는 Trp와 유사한 흡수 스펙트럼을 갖는다. 이러한 흡광도 특성을 기반으로 280 nm UV LED를 사용하여 단백질 전개 측정을 위해 Tyr 및 Trp 모두에서 형광을 여기시킬 수 있습니다.
또한 1X PBS와 0.1 M HCl/KCl에서 희석된 BSA의 형광 스펙트럼을 측정하였다(그림 1). BSA는 혈장의 주요 구성 요소이며, 체액의 적절한 분포를 유지하기 위해 삼투압의 운반 단백질 및 조절기로 기능합니다. BSA가 0.1 M HCl/KCl 용액의 낮은 pH에 노출되었을 때, 단백질의 구조가 변화하여 Trp와 Tyr 아미노산을 다른 환경에 노출시켰다.형광 스펙트럼은 1X PBS(적색 형광 곡선)에서 펼쳐진 상태(청색 형광 곡선)로 단백질이 접혀질 때 강도와 피크 형광이 더 짧은 파장으로 이동한다.
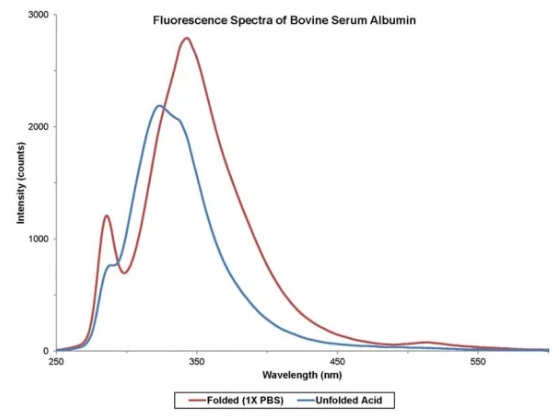
그림1 : 혈장의 주요 성분인 소 혈청 알부민의 형광 스펙트럼은 낮은 pH 완충제에 노출되어 단백질 구조의 변화를 드러낸다.
1X PBS 및 0.1 M HCl/KCl에서 희석된 리소자임에 대한 고유 단백질 형광 스펙트럼은 그림 2에 나와 있습니다. 라이소자임은 박테리아의 세포벽을 분해하는 효소이다. 이러한 측정에 사용된 리소자임은 닭알 흰자에서 분리되어 항균제 역할을 한다. 리소자임이 낮은 pH 용액에 노출되면 단백질 구조가 변화하여 트립 및 티르 아미노산을 다른 환경에 노출시킵니다.형광 스펙트럼은 단백질이 1X PBS(적색 형광 곡선)에서 접힌 형태에서 펼쳐진 상태(청색 형광 곡선)로 이동함에 따라 강도가 감소한다.
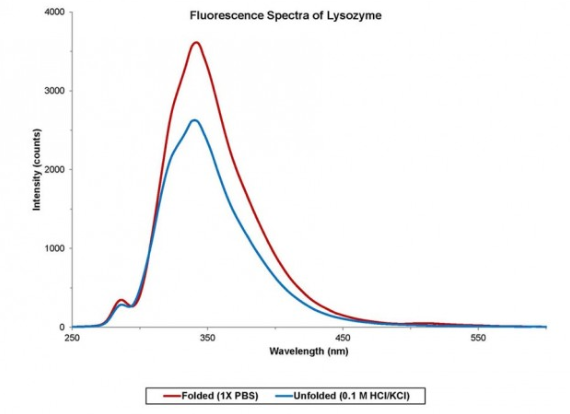
그림 2 : 낮은 pH 용액에 노출되면 리소자임 단백질 구조가 접힌 상태에서 펼쳐지는 것으로 변화합니다. 형광 측정에서 밝혀진 변형입니다.
Conclusions
BSA와 리소자임에 대해 설명된 결과는 이들 단백질에 대한 단백질 구조에 대한 훨씬 더 큰 그림의 일부입니다. 예를 들어, 구아니딘 또는 DMSO와 같은 카오 트로픽 제제는 단백질 구조에 대한보다 자세한 정보를 제공하기 위해 농도를 증가시키는 데 사용될 수 있습니다. 또한 형광을 이용한 펼침 과정을 따라 pH를 점차적으로 증가시킬 수 있다. 온도 조절 큐벳 홀더를 사용하여 샘플의 온도를 천천히 증가시킴으로써 단백질을 전개할 수 있다.
240-627 nm의 파장 범위를 커버하는 강력한 LED 여기 소스의 가용성은 단백질의 내재적 및 외재적 형광 반응을 조사할 수 있는 많은 기회를 제공합니다. 광범위한 LED 옵션은 여러 여기 파장으로 테스트할 수 있으며, 이는 연구자가 각 형광광의 형광 여기에 최적의 파장을 사용할 수 있게 합니다.UV LED를 고감도 분광계 및 유연한 샘플링 장치와 결합하면 광대한 어레이의 흡광도 및 형광 측정이 가능합니다.